金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
在体外诊断(IVD)试剂的研发与生产中,缓冲体系的稳定性直接影响检测结果的准确性与可靠性。传统Tris缓冲液配制常依赖盐酸(HCl)和氢氧化钠(NaOH)调节pH值,但二者的强腐蚀性及潜在干扰问题,给生产操作和检测性能带来挑战。Tris(三羟甲基氨基甲烷)与Tris-HCl的联合使用,凭借其独特的缓冲机制,成为规避盐酸与氢氧化钠的理想选择,在体外诊断试剂中展现出重要应用价值。
一、Tris与Tris-HCl的协同缓冲原理
Tris是一种弱碱性有机化合物,其分子结构中的氨基可与氢离子结合,形成质子化的Tris⁺;而Tris-HCl是Tris与盐酸反应生成的酸性盐,在水溶液中可解离出Tris⁺和Cl⁻。二者联合使用时,通过以下协同作用构建稳定缓冲体系:
• 当体系遭遇外源性酸性物质时,游离的Tris(弱碱)会主动结合H⁺,阻止pH值过度下降;
• 当体系引入碱性物质时,Tris-HCl解离出的Tris⁺会释放H⁺,抑制pH值大幅上升。
该缓冲对的有效pH范围为7.0-9.1,可匹配多数体外诊断反应(如抗原抗体结合、酶催化反应、核酸扩增等)所需的生理pH环境,无需额外添加盐酸或氢氧化钠调节,从根本上简化了试剂配制流程。
二、规避盐酸与氢氧化钠的核心优势
1. 提升生产操作安全性
盐酸具有强挥发性和腐蚀性,易刺激呼吸道并腐蚀设备;氢氧化钠为强碱性腐蚀剂,接触皮肤或黏膜会造成灼伤。相比之下,Tris与Tris-HCl均为性质温和的有机化合物,无强腐蚀性,可显著降低生产过程中的安全风险,减少防护设备投入和操作人员培训成本。
2. 减少对检测体系的干扰
盐酸引入的Cl⁻和氢氧化钠引入的Na⁺可能干扰检测反应:例如,高浓度Cl⁻会抑制某些酶(如辣根过氧化物酶)的活性,Na⁺可能影响胶体金颗粒的稳定性或PCR反应中DNA聚合酶的效率。Tris与Tris-HCl联合使用时,体系中仅含Tris⁺和少量Cl⁻(来自Tris-HCl的解离),成分单一且无额外离子干扰,能更精准地维持检测反应的最佳环境,提升结果的重复性。
3. 简化试剂配制工艺
传统缓冲液需通过滴加盐酸或氢氧化钠逐步调整pH值,过程中易因滴加速度不均或反应延迟导至pH波动,需反复测量和调整,耗时且难以标准化。而Tris与Tris-HCl可通过预先计算的摩尔比直接混合(如根据目标pH值,按一定的质量比或摩尔比投入固体纯品的牛莎Tris和牛莎Tris-HCL),快速达到预设pH值,减少操作步骤,便于大规模生产中的质量控制。
三、在体外诊断试剂中的具体应用场景
1. 免疫诊断试剂
在酶联免疫吸附试验(ELISA)、化学发光免疫分析(CLIA)等试剂中,Tris与Tris-HCl缓冲体系可稳定抗原、抗体的空间结构,避免其因pH波动发生变性。例如,在洗涤液和封闭液中,该体系能维持蛋白活性,减少非特异性结合,提高检测灵敏度。
2. 分子诊断试剂
在PCR、qPCR等核酸扩增试剂中,Tris-HCl可提供Taq DNA聚合酶所需的最佳pH环境(通常为8.3-8.8),同时其弱碱性可中和反应中产生的酸性物质,保证扩增效率稳定。由于无需添加氢氧化钠,避免了Na⁺对DNA聚合酶的抑制,进一步提升扩增反应的特异性。
3. 生化诊断试剂
在肝功能、肾功能等生化检测试剂中,Tris与Tris-HCl缓冲体系可保护酶与底物的反应活性。例如,检测谷丙转氨酶(ALT)时,该体系能维持反应pH在7.5左右,确保酶催化反应高效进行,减少因pH偏移导至的结果偏差。
四、应用中的关键注意事项
• 纯度选择:需使用高纯度的Tris与Tris-HCl,避免重金属离子等杂质对检测反应的干扰,尤其在分子诊断和免疫诊断中,纯度直接影响试剂的最低检测限。
• 配比精准度:通过调整Tris与Tris-HCl的摩尔比控制pH值(如目标pH=8.0时,二者摩尔比约为0.87),具体不同pH下Tris和Tris-HCL的质量比和摩尔比,可见以下:
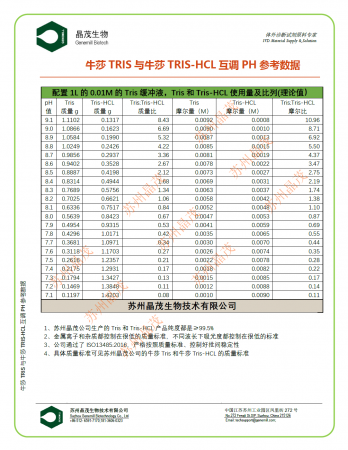
牛莎Tris和牛莎Tris-HCL互调配比
结语
Tris与Tris-HCl的联合应用,通过优化缓冲体系设计,从根源上规避了盐酸与氢氧化钠的使用局限,在提升体外诊断试剂的安全性、稳定性和生产效率方面具有不可替代的优势。随着IVD行业对试剂性能和标准化要求的不断提高,这一方案将成为缓冲体系研发的重要方向,为精准诊断提供更可靠的技术支持。
|
|
 /3
/3 